19 BAB I PENDAHULUAN 1.1 LATAR BELAKANG Istilah protein berasal dari kata Yunani Proteos, yang berarti yang utama atau yang didahulukan. Kata ini diperkenalkan oleh seorang ahli kimia belanda, Gerardus Mulder (1802-1880), karena ia berpendapat bahwa protein adalah zat yang paling penting dalam setiap organisme. Protein adalah bagian dari semua sel hidup dan merupakan bagian terbesar tubuh sesudah air. Seperlima bagian tubuh adalah protein, separuhnya ada didalam otot, seperlima didalam tulang dan tulang rawan, sepersepuluh didalam kulit, dan selebihnya didalam jaringan lain dan cairan tubuh. Semua enzim, berbagai hormon, pengangkut zat- zat gizi dan darah, matriks interseluler dan sebagainya protein. Disamping itu asam amino yang membentuk protein bertindak sebagai prekursor sebagian besar koenzim, hormon, asam nukleat, dan molekul-molekul yang esensial untuk kehidupan. Protein mempunyai fungsi khas yang tidak dapat digantikan oleh zat gizi lain, yaitu membangun serta memelihara sel-sel dan jaringan tubuh.

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript
BAB IPENDAHULUAN1.1 LATAR BELAKANG
Istilah protein berasal dari kata Yunani Proteos, yang berarti yang utama atau yang didahulukan. Kata ini diperkenalkan oleh seorang ahli kimia belanda, Gerardus Mulder (1802-1880), karena ia berpendapat bahwa protein adalah zat yang paling penting dalam setiap organisme. Protein adalah bagian dari semua sel hidup dan merupakan bagian terbesar tubuh sesudah air. Seperlima bagian tubuh adalah protein, separuhnya ada didalam otot, seperlima didalam tulang dan tulang rawan, sepersepuluh didalam kulit, dan selebihnya didalam jaringan lain dan cairan tubuh. Semua enzim, berbagai hormon, pengangkut zat-zat gizi dan darah, matriks interseluler dan sebagainya protein. Disamping itu asam amino yang membentuk protein bertindak sebagai prekursor sebagian besar koenzim, hormon, asam nukleat, dan molekul-molekul yang esensial untuk kehidupan.Protein mempunyai fungsi khas yang tidak dapat digantikan oleh zat gizi lain, yaitu membangun serta memelihara sel-sel dan jaringan tubuh.
BAB IIPEMBAHASAN
2.1 KOMPOSISI KIMIA PROTEIN
Protein adalah molekul makro yang mempunyai berat molekul antara lima ribu hingga beberapa juta. Protein terdiri atas rantai-rantai panjang asam amino yang terikat satu sama lain dalam ikatan peptida. Asam amino terdiri atas unsur-unsur karbon, hidrogen, oksigen dan nitrogen. Beberapa asam amino disamping itu mengandung unsur-unsur fosfor, besi, sulfur, iodiom, dan kobalt. Unsur nitrogen adalah unsur utama protein, karena terdapat didalam semua protein akan tetapi tidak terdapat didalam karbohidrat dan lemak. Unsur nitrogen merupakan 16% dari berat protein.Molekul protein lebih kompleks dari pada karbohidrat dan lemak dalam hal berat molekul dan keanekaragaman unit-unit asam amino yang membentuknya. Berat molekul protein bisa mencapai 40 juta. Bandingkan dengan berat glukosa yang besarnya 180. Ada dua puluh jenis asam amino yang diketahui sampai sekarang yang terdiri atas sembilan asam amino esensial ( asam amino yang tidak dapat dibuat tubuh dan harus didatangkan dari makanan ) dan sebelas asam amino nonesensial. Sumber protein berasal dari bahan makanan hewani merupakan sumber protein yang baik, dalam jumlah maupun mutu, seperti telur, susu, daging, ayam, unggas, ikan, dan kerang. Sumber protein nabati adalah gandum, jagung, kacang kedelai dan hasilnya, seperti tempe dan tahu, serta kacang-kacangan lain. Kacang kedelai merupakan sumber protein nabati yang mempunyai mutu atau nilai biologi tertinggi. Bahan makanan nabati yang kaya akan protein adalah kacang-kacangan.
2.2 PENGGOLONGAN, STRUKTUR DAN DENATURASI PROTEIN
a) Penggolongan Protein Berdasarkan Bentuk Protein globularProtein Globular berbentuk bola terdapat dalam cairan jaringan tubuh. Protein ini larut dalam air, berdifusi cepat dan bersifat dinamis, mudah berubah dibawah pengaruh suhu, konsentrasi garam serta mudah mengalami denaturasi. Contohnya meliputi enzim, hormon dan protein darah. Protein serabut (fibrous)Terdiri atas beberapa rantai peptida berbentuk spiral yang terjalin satu sama lain sehingga menyerupai batang yang kaku. Protein fibrous mempunyai bentuk molekul panjang seperti serat atau serabut, tidak larut dalam air. mempunyai kekuatan mekanis yang tinggi dan tahan terhadap enzim pencernaan. Protein ini terdapat dalam unsur-unsur struktur tubuh. Contohnya meliputi kolagen, myosin, fibrin, dan karatin pada rambut, kuku, dan kulit.b) Struktur ProteinAda 4 struktur protein antara lain ;1) Struktur PrimerStruktur primer adalah rantai polipeptida. Struktur primer protein di tentukan oleh ikatan kovalen antara residu asam amino yang berurutan yang membentuk ikatan peptida. Struktur primer dapat di gambarkan sebagai rumus bangun yang biasa di tulis untuk senyawa organik.2) Struktur SekunderStruktur sekunder ditentukan oleh bentuk rantai asam amino : lurus, lipatan, atau gulungan yang mempengaruhi sifat dan kemungkinan jumlah protein yang dapat dibentuk. Struktur ini terjadi karena ikatan hydrogen antara atom O dari gugus karbonil ( C=O) dengan atom H dari gugus amino ( N-H ) dalam satu rantai peptida, memungkinkan terbentuknya konfirasi spiral yang disebut struktur helix. Heliks AlfaRantai utama polipeptida pada suatu heliks alpha berpuntir sama besarnya mengelilingi masing-masing karbon alpha dengan sudut phi sekitar -57 derajat dan sudut psi sekitar -47 derajat. Satu putaran sempurna heliks mengandung rata-rata 3,6 residu aminoasil, dan jarak per putaran (pitchnya) adalah 0,54 nm. Gugus R pada masing-masing residu aminoasil dalam sebuah heliks alpha menghadap keluar. Protein hanya mengandung asam L amino, dengan heliks alpha kinan (right handed) sebagai heliks yang lebih stabil, dan hanya heliks alpha kinan yang terdapat di protein. Diagram skematis protein memperlihatkan heliks alpha sebagai silinder. Stabilitas suatu heliks alpha terutama disebabkan oleh ikatan hidrogen yang terbentuk antara oksigen pada karbonil ikatan peptide dan atom hidrogen pada nitrogen ikatan peptida residu keempat di sebelah hilir rantai polipeptida. Kemampuan untuk membentuk ikatan hidrogen dalam jumlah maksimal, yang diperkuat oleh interaksi van der Waals di bagian inti pada struktur yang terkemas rapat ini, merupakan kekuatan pendorong termodinamik bagi terbentuknya heliks alpha. Karena nitrogen ikatan peptida pada prolin tidak memiliki sebuah atom hidrogen untuk disumbangkan ke ikatan hidrogen, prolin hanya dapat diakomodasikan secara stabil pada putaran pertama heliks alpha. Jika berada di tempat lain, prolin mengganggu konformasi heliks. Karena ukurannya yang kecil, glisin juga sering menyebabkan penekukan di heliks alpha. Banyak heliks alpha memiliki gugus R yang dominan hidrofobik di salah satu sisi sumbu dan dominan hidrofilik di sisi yang lain. Heliks amfifatik ini beradaptasi baik terhadap pembentukan pertemuan antara region polar dan nonpolar, misalnya bagian interior protein yang hidrofobik dengan lingkungan airnya. Kelompok-kelompok heliks amfifatik dapat menciptakan suatu kanal, atau pori yang memungkinkan molekul polar tertentu menembus membran sel hirofobik.
Lembar Beta ( Beta Sheet )Struktur sekunder reguler kedua (karena itu diberi nama beta) yang dapat dikenali dalam protein adalah lembar beta (beta sheet). Residu-residu asam amino pada lembar beta, jika dilihat dari tepi, membentuk pola zigzag atau lipatan dengan gugus R residu-residu berdekatan yang mengarah berlawanan. Tidak seperti rantai uatam pada heliks alpha yang padat, tulang punggung peptida pada lembar beta sangat melebar. Tetapi, seperti heliks alpha, stabilitas lembar beta terutama disebabkan oleh ikatan hidrogen antara oksigen karbonil dan hidrogen amida ikatan peptida. Namun, berbeda dengan heliks alpha, ikatan-ikatan ini terbentuk dengan segmen-segmen lembar beta yang berdekatan.Lembar-lembar beta yang saling berinteraksi dapat tersusun membentuk lembar beta pararel, dengan segmen-segmen rantai polipeptida berdekatan yang memiliki arah amino ke karboksil yang sama, atau lembar antipararel, yang segmen-segmennya tersebut berjalan dalam arah berlawanan. Kedua konfigurasi ini memungkinkan terbentuknya jumlah ikatan hidrogen yang maksimal antara segmen-segmen, atau unati lembar tersebut. Sebagian besar lembar beta tidaklah benar-benar datar, tetapi cenderung agak terpuntir ke kanan. Kelompok-kelompok untai lembar beta yang terpuntir membentuk inti banyak protein globural. Diagram sekamatis menggambarkan lembar beta sebagai tanda panah yang menunjukkan arah amino ke terminal karboksil.
Gelungan & Tekukan Sekitar separuh residu pada protein globural tipikal terletak di heliks alpha dan lembar beta dan seprauh di gelungan (loops), belokan (turn), tekukan (bends), dan fitur konformasi tambahan lainnya. Belokan dan tekukan merujuk pada segmen pendek asam amino yang menyatukan dua unit struktur sekunder, misalnya dua untai lembar beta antipararel yang berdekatan. Belokan beta melibatkan empat residu aminoasil, yang residu pertamanya berhubungan melalui ikatan hidrogen ke residu keempat sehingga terbentuk suatu belokan tajam 180 derajat. Prolin dan glisin sering terdapat di belokan beta. Gelungan adalah region yang mengandung residu melebihi jumlah minimal yang diperlukan untuk menghubungkan regio-regio yang berdekatan pada struktur sekunder. Gelungan yang konformasinya ireguler memiliki peran biologis penting. Pada banyak enzim, gelungan yang menjembatani domain-domain yang berperan dalam pengikatan substrat sering mengadung residu aminoasil yang ikut serta dalam katalisis. Pada protein pengikat DNA, misalnya represor dan faktor transkripsi, motif heliks-gelungan-heliks membentuk bagian pengikat oligonukleotida. Motif struktural, misalnya motif heliks-gelungan-heliks yang berada di antara struktur sekunder dan tersier sering dinamai struktur supersekunder. Karena terletak di permukaan protein sehingga terpajan oleh pelarut, banyak gelungan dan tekukan membentuk bagian yang mudah diakses, atau epitop untuk pengenalan dan pengikatan antibody. Meskipun tidak memiliki regulitas struktural yang jelas, namun gelungan terdapat dalam konformasi spesifik yang distabilkan melalui ikatan hidrogen, jembatan garam, dan interaksi hidrofobik dengan bagian lain protein. Namun, tidak semua bagian protein selalu teratur. Protein dapat mengandung bagian-bagian yang berantakan, sering di terminal amino atau karboksil ekstrem dan ditandai oleh fleksibilitas konformasi yang tinggi. Pada banyak keadaan, bagian yang berantakan ini menjadi teratur setelah berikatan dengan ligar. Fleksibilitas strktural ini memungkinkan bagian ini bekerja sebagai tombol pengendali ligan yang memengaruhi struktur dan fungsi protein.
3) Struktur tersierStruktur tersier ditentukan oleh ikatan tambahan antara gugus R pada asam-asam amino yang memberi bentuk tiga dimensi sehingga membentuk struktur kompak dan padat suatu protein.1) Residu asam amino hidrofobik cenderung untuk menempati dan berkelompok dalam interior dari protein globular, dimana mereka menjauhi air, sedangkan residu hidrofilik biasanya terdapat pada permukaan, dimana mereka berinteraksi dengan air.2) Tipe interaksi non kovalen antara residu asam amino yang menghasilkan bentuk tiga dimensi dari protein termasuk interaksi hidrofobik, interaksi elektrostatik (ionic), ikatan hidrogen dan interaksi van der Waals. 3) Semua informasi yang diperlukan untuk protein secara bebas menganggap struktur tersier dinyatakan oleh urutan primernya. Kadang-kadang moleku yang dikenal sebagai chaperones (protein pendamping ) berinteraksi dengan polipeptida untuk membantu memperoleh struktur yang benar. Protein seperti itu baik mangatalisis laju perlipatan atau melindungi protein dari terbentuknya kekacauan intra molokuler yang nonproduktif selama pelipatan.4) Struktur kuartenerStruktur kuartener adaalah susunan kompleks yang terdiri dari dua rantai polipeptida atau lebih, yang setiap rantainya bersama dengan struktur primer, sekunder, tersier membentuk satu molekul protein yang besar dan aktif secara biologis.Istilah struktur tersier merujuk pada konformasi tiga dimensi keseluruhan suatu polipeptida. Dalam ruang tiga dimensi, struktur ini menunjukkan bagaimana gambaran struktur sekunder-heliks, lembaran,tekukan,belokan, dan gelungan-tersusun membentuk domain dan bagaimana domain-domain ini berhubungan satu sama lain dalam ruang. Domain adalah suatu bagian dari struktur protein yang mampu melakukan tugas kimia atau fisika tertentu, misalnya mengikat substrata tau ligan lain. Domain lain dapat berfungsi menghubungkan protein dengan membrane atau berinteraksi dengan molekul regulatorik yang memodulasi fungsi protein tersebut. Suatu polipeptida kecil misalnya triosa fosfat isomerase atau mioglobin dapat mengandung suatu domain. Protein kinase mengatalisis pemindahan sebuah gugus fosforil dari ATP ke peptida atau protein. Bagian terminal amino pada polipeptida, yang kaya akan lembar beta, mengikat ATP, sementara domain terminal karboksil, yang kaya akan heliks alpha, mengikat peptida atau substrat protein. Gugus yang mengatalisis pemindahan fosforil terletak di gelungan yang berada di pertemuan kedua domain.
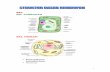
Gambar disamping; gambar Struktur protein, 1) struktur primer, 2) strutur sekunder, 3) struktur tersier, 4) struktur kuarterner.2341
c) Denaturasi Protein Protein dapat mempertahankan kesesuaian bentuknya asalkan lingkungan fisik dan kimianya dipertahankan. Jika lingkungan berubah maka, protein dapat terurai atau mengalami perubahan sifat ( denaturasi ) mereka dapat kehilangan struktur sekunder, tersier, dan kuarternya sehingga aktivitas biologisnya juga hilang.1) Kesesuaian bentuk protein bergantung pada ikatan hidrogen, yang lemah dan sangat senitif terhadap perubahan PH dan suhu.2) Paparan singkat pada suhu yang tinggi ( diatas 60oC ) atau paparan pada asam atau basa kuat dalam periode waktu yang lama akan menyebabkan denaturasi karena ikatan hidrogen ruptur.Sebagian protein dapat dikembalikan kebentuk aslinya, jika terdenaturasi tanpa harus menjadi insoluble. Perbedaan panas yang besar dapat menyebabkan denaturasi yang menetap. Putih telur akan memadat dan menjadi insoluble jika dipanaskan. Suhu tubuh yang sangat tinggi dapat menyebabkan koagulasi protein selular. Jika suhu tubuh naik sampai diatas 41oC atau 42oC maka akan mengakibatkan denaturasi protein.Jika suatu protein yang terdenaturasi kembali ke keadaan alamiahnya setelah agen yang mengalami denaturasi disingkirkan, proses tersebut disebut renaturasi.
2.3 ASAM AMINOAsam amino terdiri atas atom karbon yang terikat pada suatu gugus karboksil ( - COOH ) satu gugus amino ( - NH2 ), satu atom hidrogen ( - H ) dan satu gugus radikal ( - R ), atau rantai cabang. Sebagaimana tampak pada gambar struktur asam amino dibawah ini ; COOH (gugus karboksil)H C R (gugus radikal)NH2 (gugus amino)a) Klasifikasi Asam Amino1) Asam amino mengandung sedikitnya satu gugus asam Karboksil (-COOH) dan sedikitnya satu gugus amino (-NH2) kedua gugus tersebut tersebut terikat pada atom karbon yang sama. Setiap asam amino mempunyai anak rantai yang disebut sebagai satu gugus R. a) Asam-asam amino memiliki perbedaan dalam gugus R-nya yang memberi ciri khas dan mempengaruhi sifat protein tempat asam amino tersebut bergabung.b) Gugus R nonpolar menyebabkan asam amino relatif tidak larut dalam air. Gugus R yang polar atau bermuatan listrik menyebabkan asam amino larut dalam air.2) Asam-asam amino bergabung untuk membentuk protein melalui reaksi kondensasi (dehidrasi) antara gugus karboksil dari salah satu asam amino dan gugus amino dari asam amino lain.
b) Klasifikasi Asam Amino Menurut Esensial dan Tidak EsensialDr. William Rose, (1917) seorang peonir dalam penelitian protein dengan menggunakan berbagai campuran asam amino dan meneliti pengaruhnya pertumbuhan tikus percobaan dan manusia. membagi asam amino dalam dua golongan, yaitu asam amino esensial dan tidak esensial. dalam penelitiannya ternyata ada 10 macam asam amino yang dibutuhkan binatang ( tikus ) untuk pertumbuhan yang tidak dapat disintesis tubuh , asam amino ini dinamakan asam amino esensial. Asam amino lain dinamakan asam amino tidak esensial. Asam amino tidak esensial juga penting untuk pembentukan protein tubuh, tetapi asam amino ini bila tidak terdapat dalam tubuh dapat disintesis tubuh dalam jumlah yang diperlukan. Ternyata ada sembilan jenis asam amino esensial untuk manusia yang diperlukan untuk pertumbuhan dan pemeliharaan jaringan tubuh. kesembilan asam amino ini tidak dapat disintesis tubuh, yang berarti harus ada dalam makanan sehari-hari. Bila tubuh mengandung cukup nitrogen, tubuh mampu mensintesis sebelas jenis asam amino lain, yaitu asam amino tidak esensial yang diperlukan untuk pertumbuhan dan pemeliharaan jaringan tubuh. Nitrogen ini dapat berasal dari asam amino tidak esensial dan asam amino esensial yang berlebihan. Sudah tentu ke 20 asam amino tersebut diperlukan untuk pertumbuhan, perkembangan dan pemeliharaan kesehatan tubuh.Tabel. Pengelompokan asam aminoNamaSingkatanRumusR
A. Asam amino dengan sebuah gugus amino dan karboksil
1. GlisinGly
2. AlaninAla
R = H atau alkil
3. ValinVal
4. LeusinLeu
5. IsoleusinIle*
6. SerinSer
R mengandung sebuah gugus fungsi alkohol
7. TreoninThr*
8. SisteinCys
Dua buah asam amino mengandung belerang
9. MetioninMet*
10. ProlinPro
Gugus amino sekunder dan berbentuk cincin
11. FenilalaninPhe*
12. TirosinTyr
13.TriptofanTrp*
B. Asam amino dengan sebuah gugus amino dan dua buah gugus karboksil
14. Asam aspartatAsp
15.asam glutamatGlu
16. asparaginAsn
17. GlutaminGln
C. Asam amino dengan sebuah gugus karboksil dan dua buah gugus basa
18. LisinLys*
19. ArgininArg
20. HistidinHis
2.4 FUNGSI PROTEIN
1. Sebagai biokatalisator (enzim). 2. Sebagai protein transport contohnya hemoglobin mengangkut oksigen dalam eritrosit, mioglobin mengangkut oksigen dalam otot. Ion besi diangkut dalam plasma darah oleh transferin dan disimpan dalam hati sebagai kompleks dengan feritin.3. Sebagai pengatur pergerakan. Protein merupakan komponen utama daging. Gerakan otot terjadi karena ada dua molekul (aktin dan miosin) protein yang saling bergeseran. Pergerakan silia dan flagela pada organisme protista akibat dari protein tubulli pada organel tersebut. 4. Sebagai penunjang mekanis. Kekuatan dan daya tahan robek kulit dan tulang disebabkan adanya kolagen. Pada persendian ada elastin. Pada kuku, bulu rambut ada protein keratin.5. Pertahanan tubuh dalam bentuk antibodi. Suatu protein khusus yang mengikat benda asing yang masuk kedalam tubuh seperti virus, bakteri dan lain lain.6. Sebagai media perambatan impuls saraf. Protein ini biasanya berbentuk reseptor misalnya rodopsin suatu protein yang bertindak sebagai reseptor atau penerima warna atau cahaya pada sel sel mata.7. Sebagai pengendalian pertumbuhan. Protein bekerja sebagai reseptor yang dapat mempengaruhi fungsi bagian bagian DNA yang mengatur sifat dan karakter.
2.5 PENCERNAAN DAN METABOLISME PROTEIN
a) Pencernaan ProteinSebagian besar protein dicernakan menjadi asam amino, selebihnya menjadi tripeptida dan dipeptida. Lambung Pencernaan atau hidrolisis protein dimulai didalam lambung. Asam klorida lambung membuka gulungan protein (proses denaturasi), sehingga enzim pecernaan dapat memecah ikatan peptida. Asam klorida mengubah enzim pepsinogen tidak aktif yang dikeluarkan oleh mukosa lambung menjadi bentuk aktif pepsin. Karena makanan hanya sebentar tinggal di lambung, pencernaan protein hanya terjadi hingga dibentuknya campuran polipeptida, proteose dan pepton. Usus halus Pencernaan protein dilanjutkan didalam usus halus yang berasal campuran enzim proteose. Pankreas mengeluarkan cairan yang bersifat sedikit basa dan mengandung berbagai prekursor protease seperti tripsinogen, kemotripsinogen, prokarbobsipeptidase, dan proelastase. Enzim-enzim ini menghidrolisis ikatan peptida tertentu. Sentuhan kimus terhadap mukosa usus halus mengrangsang dikeluarkannya enzim enterokinase yang mengubah tripsinogen tidak aktif yang berasal dari pankreas menjadi Tripsin aktif. Perubahan ini juga dilakukan oleh Tripsin sendiri secara oto-katalitik disamping itu Tripsin dapat mengaktifkan enzim-enzim proteolitik lain berasal dari pankreas. Kimotripsinogen diubah menjadi beberapa jenis kimotripsin aktif; prokarboksipeptidase dan proelastase diubah menjadi karboksipeptidase dan elastase aktif. Enzim-enzim pankreas ini memecah protein dari polipeptida menjadi peptida lebih pendek, yaitu tripeptida, dipeptida, dan sebagian menjadi asam amino. Mukosa usus halus juga mengeluarkan enzim-enzim proteose yang menghidrolisis ikatan peptida. Sebagian enzim mukosa usus halus ini bekerja di dalam sel.Hasil pencernaan terjadi setelah memasuki sel-sel mukosa atau pada saat diangkut pada dinding epitel. Mukosa usus halus mengeluarkan enzim amino peptidase yang memecah polipeptida menjadi asam amino bebas. Enzim ini membutuhkan mineral Mn++ dan Mg++ untuk pekerjaannya. Mukosa usus halus juga mengandung enzim dipeptidase yang memecah dipeptida tertentu dan membutuhkan mineral Co++ dan Mn++ untuk pekerjaannya.
Ringkasan pencernaan proteinSaluran pencernaanPencernaan dan absorpsi
1. MulutMengunyah makanan bercampur dengan air ludah dan ditelan.
2. EsofagusTidak ada pencernaan
3. LambungAsam lambung membuka molekul protein dan mengaktifkan enzim lambung.
4. Usus halusProtein protease lambung HCL polipeptida lebih pendek Pepsin ( proteose dan pepton )Polipeptida protease pankreas dipeptida, tripeptida dan Eterokinase, tripsin asam amino ( diserap )Peptida dipeptidase dan asam amino bebas Tripeptidase mukosa usus halus ( diserap )
b) Metabolisme Protein
a) Absorpsi dan TransportasiHasil akhir pencernaan protein terutama berupa asam amino dan ini segera diabsorpsi dalam waktu lima belas menit setelah makan. Absorpsi terutama terjadi dalam usus halus berupa empat sistem absorpsi aktif yang membutuhkan energi. Asam amino yang diabsorpsi memasuki sirkulasi darah melalui vena porta dan dibawa ke hati. Sebagian asam amino digunakan oleh hati, dan sebagian lagi melalui sirkulasi darah di bawa ke sel-sel jaringan. Kadang-kadang protein yang belum dicerna dapat memasuki mukosa usus halus dan muncul dalam darah. Hal ini sering terjadi pada protein susu dan protein telur yang dapat menimbulkan gejala alergi (immunological sensitive protein ).Sebagian besar asam amino telah diabsorpsi pada saat asam amino sampai di ujung usus halus. Hanya 1% protein yang dimakan ditemukan dalam feses. Protein endogen yang berasal sekresi saluran cerna dan sel-sel yang rusak juga dicerna dan diabsorpsi.
b) Katabolisme proteinKatabolisme protein (penguraian asam amino untuk energi) berlangsung di hati. Jika sel telah mendapatkan protein yang mencukupi kebutuhannya. Setiap asam amino tambahan akan dipakai sebagai energi atau disimpan sebagai lemak.1. Deaminasi Asam AminoDeaminasi asam amino merupakan langkah pertama, melibatkan pelepasan satu hidrogen dan satu gugus amino sehingga membentuk amonia (NH3). Amonia yang bersifat racun akan masuk ke peredaran darah dan dibawa ke hati. Hati akan mengubah amonia menjadi ureum yang sifat racunnya lebih rendah, dan mengembalikannya ke peredaran darah. Ureum dikeluarkan dari tubuh melalui ginjal dan urine. Ureum diproduksi dari asam amino bebas didalam tubuh yang tidak digunakan dan dari pemecahan protein jaringan tubuh.2. Osidasi asam amino terdeaminasiBagian asam amino nonitrogen yang tersisa disebut produk asam keto yang teroksidasi menjadi energi melalui siklus asam nitrat. Beberapa jenis asam keto dapat diubah menjadi glukosa (glukoneogenesis) atau lemak (lipogenesis) dan disimpan didalam tubuh.Karbohidrat dan lemak adalah cadangan protein dan dipakai tubuh sebagai pengganti protein untuk energi. Sat kelaparan, tubuh menggunakan karbohidrat dan lemak baru kemudian memulai mengkatabolis protein.
c) Anabolisme protein1. Sintesis proteinSintesis protein dari asam amino berlangsung disebagian sel tubuh. Asam amino bergabung dengan ikatan peptida pada rangkaian tertentu yang ditentukan berdasarkan pengaturan gen.Sintesis protein meliputi pembentukan rantai panjang asam amino yang dinamakan rantai peptida. Ikatan kimia yang mengaitkan dua asam amino satu sama lain dinamakan ikatan peptida. Ikatan ini terjadi karena satu hidrogen (H) dari gugus amino suatu asam amino bersatu dengan hidroksil (OH) dari gugus asam karboksil asam amino lain. Proses ini menghasilkan satu molekul air, sedangkan CO dan NH yang tersisa akan membentuk ikatan peptida . sebaliknya, ikatan peptida ini dapat dipecah menjadi asam amino oleh asam atau enzim pencernaan dengan penambahan satu molekul air, proses ini dinamakan hidrolisis.2. TransaminasiTransaminasi yang berlangsung di hati, merupakan sintesis asam amino nonesensial melalui pengubahan jenis asam amino menjadi jenis lainnya. Proses ini melibatkan pemindahan satu gugus amino (NH2) dari sebuah asam amino menjadi satu asam keto sehingga terbentuk satu asam amino dan satu asam keto baru.
BAB IIIPENUTUP
3.1 KESIMPULAN
Protein adalah molekul makro yang mempunyai berat molekul antara lima ribu hingga beberapa juta. Protein terdiri atas rantai-rantai panjang asam amino yang terikat satu sama lain dalam ikatan peptida. Penggolongan protein berdasarkan bentuknya yaitu 1) protein globular, 2) protein serabut (fibrous). Dan struktur protein terdiri ; protein primer, protein sekunder, protein tersier, dan protein kuartener.Fungsi protein antara lain ; Sebagai biokatalisator (enzim), Sebagai protein transport, Sebagai pengatur pergerakan, Sebagai penunjang mekanis, Pertahanan tubuh dalam bentuk antibodi, Sebagai media perambatan impuls saraf, Sebagai pengendalian pertumbuhan. Dan pencernaan protein, yaitu dari mulut, lambung, dan usus halus. Metabolisme protein terdiri dari absorpsi dan transportasi protein, katabolisme protein, dan anabolisme protein.
DAFTAR PUSTAKA
Murray, Robert K. Daryl K. Granner. Victor W. Radwell. 2009. Biokimia Harper Edisi 27. Jakarta: Penerbit Buku Kedokeran (EGC)
Sloane, Ethel.2003. Anatomi Dan Fisiologi Untuk Pemula. Jakarta: Penerbit Buku Kedokteran (EGC)
STRUKTUR PROTEIN 19
Related Documents