Diferensiasi Human Umbilical Cord Blood Stem Cell (HUCB Stem Cell) menjadi Neural Progenitor Cell (NPC) dengan Induksi Nerve Growth Factor (NGF) in vitro BAB I PENDAHULUAN A. Latar Belakang Masalah Penyakit akibat kerusakan sel saraf pada Susunan Saraf Pusat (SSP) masih merupakan masalah kesehatan di dunia dengan angka kesakitan dan kematian yang cukup tinggi. Di Amerika penyakit yang diakibatkan oleh trauma otak dan cidera medula spinalis menyerang 1,4 juta jiwa setiap tahunnya. Sebuah studi di 9 negara menunjukan insidensi stroke yang tinggi yaitu sekitar 0,1 – 0,3 per seribu individu pada usia kurang dari 45 tahun. Di Indonesia prevalensi penyakit stroke diperkirakan mencapai 500.000 per tahun dengan angka kematian mencapai 125.000 dan sisanya mengalami cacat ringan dan berat Manifestasi klinik yang timbul akibat trauma sel saraf pada penyakit-penyakit tersebut diperantarai oleh proses nekrosis maupun apoptosis sel-sel saraf (Rodriguez et al., 2008; Rashef et al., 2007; Feigin et al., 2003, Yastroki, 2006). Pasca trauma sel saraf, siklus sel akan diaktifkan kembali sebagai upaya menstimulasi proses regenerasi sel- sel tersebut. Akan tetapi, pada orang dewasa sel-sel 1

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

Diferensiasi Human Umbilical Cord Blood Stem Cell (HUCB Stem Cell) menjadi
Neural Progenitor Cell (NPC)
dengan Induksi Nerve Growth Factor (NGF) in vitro
BAB I
PENDAHULUAN
A. Latar Belakang Masalah
Penyakit akibat kerusakan sel saraf pada Susunan Saraf Pusat (SSP) masih
merupakan masalah kesehatan di dunia dengan angka kesakitan dan kematian yang
cukup tinggi. Di Amerika penyakit yang diakibatkan oleh trauma otak dan cidera
medula spinalis menyerang 1,4 juta jiwa setiap tahunnya. Sebuah studi di 9 negara
menunjukan insidensi stroke yang tinggi yaitu sekitar 0,1 – 0,3 per seribu individu
pada usia kurang dari 45 tahun. Di Indonesia prevalensi penyakit stroke diperkirakan
mencapai 500.000 per tahun dengan angka kematian mencapai 125.000 dan sisanya
mengalami cacat ringan dan berat Manifestasi klinik yang timbul akibat trauma sel
saraf pada penyakit-penyakit tersebut diperantarai oleh proses nekrosis maupun
apoptosis sel-sel saraf (Rodriguez et al., 2008; Rashef et al., 2007; Feigin et al., 2003,
Yastroki, 2006). Pasca trauma sel saraf, siklus sel akan diaktifkan kembali sebagai
upaya menstimulasi proses regenerasi sel-sel tersebut. Akan tetapi, pada orang
dewasa sel-sel saraf matur yang teraktivasi pasca trauma sel saraf memiliki
kecenderungan untuk mengalami proses apoptosis daripada proliferasi. Selain itu,
produksi sitokin proinflamasi yang berlebihan pada lokasi kerusakan dapat
menyebabkan hambatan regenerasi sel saraf. Dengan demikian proses perbaikan sel-
sel saraf setelah kerusakan merupakan hal yang sulit dilakukan secara otonom
(Byrnes et al., 2007; Yiu et al., 2006).
Chen et al (2005) melaporkan bahwa transplantasi Human Umbilical Cord
Blood stem cell (HUCB stem cell) merupakan suatu terapi yang efektif bagi
regenerasi kerusakan sel saraf. Hal ini berkaitan dengan kemampuannya dalam
meningkatkan perbaikan fungsional pasca stroke. Sejalan dengan Chen (2005),
1

penelitian yang dilakukan oleh Goldman (2006) menunjukkan bahwa HUCB stem
cell dapat memperbaiki kerusakan sel saraf pada hewan coba dengan trauma otak dan
cidera medula spinalis. Berbagai studi tersebut telah menunjukkan efek tropik
kemampuan HUCB stem cell sebagai terapi pengganti kerusakan sel karena proses
patologis. Telah diidentifikasi bahwa efek tropik stem cell ini berkaitan dengan fraksi
mononuklear dari umbilical cord blood stem cell (Maslov et al., 2004; Pesce et al.,
2003). Chen et al (2005) dan Lommatzsach et al (2005) telah mengidentifikasi bahwa
salah satu fraksi mononuklear dari HUCB stem cell, yaitu floating fraction
merupakan subfraksi yang mampu mengekpresikan protein sel saraf.
Kultur fraksi floating HUCB stem cell dengan beberapa growth factor,
antara lain Retinoic Acid (RA), Nerve Growth Factor (NGF), Brain Derived Nerve
Factor (BDNF), dan Endothelial Growth Factor (EGF) menujukkan kemampuan
diferensiasi stem cell menjadi sel saraf matur. Dalam hal ini, NGF dinilai sebagai
growth factor yang spesifik bagi diferensiasi dan pematangan neural progenitor cell
(NPC) secara in vitro maupun in vivo (Edling et al., 2004; Lee et al., 2002; Wichterle,
2002). Keberhasilan diferensiasi ini ditunjukkan dengan ekspresi beberapa marker
protein sel saraf spesifik seperti nestin, TuJ1, MAP-2 (microtubule-assosiated-
protein-2), GFAP (Glial Fibrilary Acidic Protein), trKC (Tyrosin-kinase-C), dan
molekul adesi E-NCAM (embryonic neuronal adhesion molecule). Masing-masing
marker tersebut spesifik untuk menandakan tahap diferensiasi sel saraf, dimana
ekspresi nestin mengindikasikan terbentuknya early neural cell, GFAP
mengindikasikan terbentuknya sel glia, TUJ1 mengindikasikan terbentuknya sel saraf
matur, dan trKC mengindikasikan terbentuknya faktor neurotropik (Nguyen et al.,
2004).
Locatelli et al (2003) menyatakan bahwa belum terdapat metode
transplantasi HUCB stem cell yang paling tepat untuk memperbaiki kerusakan sel
saraf pada sistem saraf pusat. Dalam hal ini, transfusi intravena dinilai sebagai
metode yang lebih baik karena kurang invasif. Namun, metode transfusi intravena ini
berisiko menimbulkan teratoma pada transfusi stem cell yang belum berdiferensiasi.
Sampai saat ini, terdapat beberapa penelitian yang mencoba melakukan transfusi
2

fraksi mononuklear stem cell untuk memperbaiki kerusakan sel saraf pasca stroke
(Nayak, 2008). Namun beberapa penelitian tersebut menunjukkan bahwa tidak
terdapat perbaikan yang nyata dari sel saraf karena kegagalan stem cell untuk
beradaptasi dengan lingkungan neurogenik (Sohur, 2008).
Drucker (2004) melaporkan bahwa kultur NPC yang diambil dari
subventrikular zone hewan coba telah berhasil ditransplantasikan kembali secara
intravena dan mampu beradaptasi dengan baik pada lingkungan neurogenik. Hal ini
mengindikasikan bahwa transplantasi stem cell dalam bentuk sel progenitor dapat
meminimalkan terjadinya teratoma. Akan tetapi, kultur NPC pada manusia
merupakan hal yang sulit untuk dilakukan karena isolasi NPC dari zona
subvenrtikular dan gyrus dentatus otak manusia melibatkan proses invasif seperti
kraniotomi. Dalam hal ini, induksi HUCB stem cell dengan berbagai growth factor in
vitro dapat menjadi alternatif sumber NPC. Studi yang dilakukan oleh Goldman
(2006) Nayak (2008) Lee et al (2002) Wichterle (2002) melaporkan bahwa untuk
mendapatkan sel saraf matur dibutuhkan rata-rata 30 hari kultur HUCB stem cell
dengan induksi berbagai growth factor. Namun, dalam studi tersebut belum
dilaporkan profil marker sel saraf pada proses diferensiasi HUCB stem cell mulai dari
pembentukan NPC sampai pematangan sel saraf.
Atas dasar pemikiran tersebut kami mengajukan proposal penelitian
mengenai diferensiasi HUCB stem cell menjadi Neural Progenitor Cell (NPC)
dengan induksi Nerve Growth Factor berdasarkan ekspresi marker protein nestin,
TuJ1, GFAP, trkC in vitro. Studi awal ini diharapkan dapat memberikan gambaran
tentang perkembangan sel saraf, khususnya sel progenitor neural dari HUCB stem cell
sehingga dapat menjadi salah satu alternatif pemecahan masalah yang berkaitan
dengan metode transplantasi stem cell. Selain itu penelitian ini juga akan
membandingkan efektivitas kadar NGF yang digunakan untuk menginduksi
diferensiasi HUCB stem cell menjadi NPC sehingga dapat meningkatkan efisiensi
penggunaan NGF tersebut dalam kultur.
3

B. Rumusan Masalah Penelitian
Masalah yang kami angkat dalam penelitian ini adalah :
Bagaimana ekspresi marker protein nestin, GFAP, TuJ1, dan trkC pada induksi
HUCB stem cell menjadi NPC dengan berbagai konsentrasi NGF in vitro berdasarkan
lama induksi?
C. Tujuan Penelitian
Tujuan dari penelitian ini adalah :
Mengetahui dan menganalisis ekspresi marker protein nestin, GFAP, TuJ1, dan trkC
pada induksi HUCB stem cell menjadi NPC dengan berbagai konsentrasi NGF in
vitro berdasarkan lama induksi.
D. Luaran yang Diharapkan
Hasil yang diharapkan dari penelitian ini adalah waktu induksi HUCB stem cell
menjadi NPC dengan berbagai konsentrasi NGF in vitro.
E. Manfaat Penelitian
Manfaat teoritis :
1. Memberikan sumbangsih bagi ilmu pengetahuan mengenai pengaruh waktu
induksi NGF pada kultur HUCB stem cell terhadap ekspresi marker sel saraf.
2. Sebagai pijakan bagi penelitian lanjutan yang akan mengembangkan metode
transfusi sel progenitor neural bagi terapi restoratif kerusakan saraf.
Manfaat aplikatif :
1. Membantu penentuan waktu induksi NGF yang tepat pada kultur HUCB stem cell
agar memperoleh kualitas NPC yang terbaik.
2. Membantu penentuan kadar NGF yang optimal pada kultur HUCB stem cell
menjadi NPC.
4

BAB II
TINJAUAN PUSTAKA
1. Neuron
a. Embriologi Neuron
Neural crest sebagai bakal pembentukan sel-sel neuron pertama kali
ditemukan pada tepi lateral neural plate setelah fase gastrula. Pembentukan
ektoderm dan mesoderm yang berasal dari neural crest dimulai setelah penutupan
dorsal neural tube pada seluruh bagian embrio. Neural crest akan berdiferensiasi
menjadi berbagai macam sel diantaranya sel neuron dan sel glia pada Susunan
Saraf Tepi (SST), sel melanosit pada kulit, sel fibroblas pada jaringan ikat, dan
beberapa sel endokrin. Saat ini telah ditemukan beberapa gen yang mempengaruhi
diferensiasi dan migrasi dari neural crest, diantaranya adalah BMP4 (Bone
Morphogenic Protein 4) yang berperan dalam penentuan aksis vertikal neural tube,
Wnt3 (Wingless-type MMTV integration site family, member 3) yang berperan
dalam segmentasi neural crest serta Sox10 (Sex determining region-Y-box 10)
yang berperan dalam diferensiasi spesifik neural crest (Begbie, 2008; Sakai and
Wakamatsu, 2005; Sarnat and Flores, 2005).
Pembentukan neurokorteks pada awal perkembangan Susunan saraf pusat
(SSP) merupakan suatu proses yang sangat kompleks. Dalam sebuah penelitian
telah dibuktikan bahwa sel-sel neuron berasal dari sel-sel progenitor yang berada
pada bagian basal telencephalon. Sel neuron yang terbentuk merupakan hasil dari
proses pembelahan sel neuroepitel yang asimetris sedangkan pembelahan yang
simetris akan menghasilkan sel neuroepitel yang baru (Haubensak et al., 2003).
Pada proses neurogenesis diketahui ada dua macam tipe neuron yang
terbentuk yaitu interneuron yang berperan dalam koneksi lokal antar sel neuron
dan neuron proyeksi yang berperan dalam perkembangan akson intrakortikal,
subkortikal dan subserebral. Interneuron yang mengandung GABA (Gamma
Amino Butyric Acid) berasal dari sel-sel progenitor telencephalon ventral
5

sedangkan neuron proyeksi yang terdiri atas neuron-neuron glutamanergik berasal
dari sel-sel progenitor dinding dorsolateral telencephalon (Molyneaux et al., 2007).
b. Biologi Neuron
Perkembangan neurogenesis pada otak yang normal dikontrol oleh
siklus sel melalui interaksi beberapa faktor seperti cyclins, CDKs (Cyclin-
Activated Kinases) dan CDKIs (Cyclin Dependent Kinase Inhibitors). Proses
tersebut akan mengatur mitosis neuroblast sampai pada tahap tertentu. Secara
umum, sel-sel yang telah berdiferensiasi seperti halnya sel neuron yang telah
matur tidak akan mengalami siklus sel untuk berproliferasi kembali. Hal
tersebut terjadi karena adanya beberapa penghambat endogen yang berperan
sebagai anti mitosis dan mencegah aktivasi komplek CDK/Cyclin. Beberapa
penghambat endogen untuk aktivitas CDKs diantaranya p21cip1, p27kip1 dan
p57kip2. Dari beberapa penelitian telah diketahui bahwa faktor penghambat
endogen yang ekspresinya paling banyak di otak adalah p27 (Byrnes et al.,
2007).
Pembentukan akson merupakan bentuk diferensiasi neuroblast
setelah fase mitosis sebagai penanda awal diferensiasi neuron. Proses ini
diawali oleh pembentukan APC/C (Anaphase Promoting Complex /
Cyclosome) pada neuroblast yang berfungsi memodifikasi regulator ekspresi
gen dan memulai penghancuran Id2 (Inhibitor of Differentiation-2). Rendahnya
kadar Id2 meningkatkan aktivasi kompleks protein E12-E47 yang berperan
penting dalam pembentukan akson untuk proses diferensiasi neuron spesifik.
Pada tahap tertentu pembentukan akson tersebut akan dibatasi oleh faktor
transkripsi seperti Sema3F (Semaphorin 3F), dan neural reseptor seperti
Notch1 (Notch homologue 1 translocation assosiated) sehingga
perkembangannya tidak berlebihan (Jackson, 2006).
6

2. Kerusakan sel neuron
Proses kerusakan pada sel saraf orang dewasa yang mengalami disfungsi
sangat dipengaruhi oleh mekanisme apoptosis yang terprogram. Membran sitoplasma
pada sel yang mengalami apoptosis tersebut akan menonjol dan membentuk badan
apoptosis. Fragmen badan apoptosis ini akan dieliminasi dengan cepat oleh sel-sel
fagosit di sekitarnya tanpa menimbulkan proses inflamasi. Perbedaan yang paling
mendasar pada patogenesis kerusakan sel saraf yang disebabkan trauma atau proses
patologis adalah timbulnya proses inflamasi yang berlebihan (Roth, 2002).
Secara umum mekanisme apoptosis sel saraf dibagi menjadi jalur intrinsik dan
jalur ekstrinsik. Jalur apoptosis intrinsik diperantarai oleh molekul BH3-domain yang
mempengaruhi penurunan molekul anti apoptosis seperti Bcl-2 dan Bcl-xL dan
peningkatan molekul pro apoptosis seperti Bax dan Bak. Hal tersebut menyebabkan
pelepasan sitokrom-C dari mitokondria dan menginduksi pembentukan apoptosom.
Komplek apoptosom ini selanjutnya akan menginduksi caspase-9 dan caspase-3.
Adapun jalur apoptosis ekstrinsik diaktivasi oleh pengaruh ikatan extracellular death
ligand oleh senyawa sitokin seperti TNF-α (Tumor Necrotizing Factor-α) dan fas
ligand (CD95L). Ikatan tersebut memacu pembentukan Death Inducing Signaling
Complex (DISC) yang dapat mengaktivasi caspase-8 dan pembentukan caspase-3.
Telah diketahui bahwa caspase-3 memiliki peran penting dalam menginduksi proses
apoptosis secara langsung (Rao, 2006).
Proses kerusakan sel saraf pasca trauma atau iskemi sel saraf ditandai dengan
peningkatan ekspresi protein terkait siklus sel. Induksi siklus sel pada sel-sel saraf
yang rusak tersebut akan mengaktifkan proses apoptosis sel-sel neuron dan
oligodendrosit. Selain itu siklus sel pasca kerusakan saraf akan menginduksi
proliferasi astrosit dan mikroglia dengan pelepasan faktor-faktor inflamasi. Secara
umum sel-sel yang telah berdiferensiasi dan melewati fase post mitosis seperti sel
neuron tidak akan mengalami siklus sel kembali. Bila induksi terhadap siklus sel
kembali terjadi pada sel neuron tersebut maka cenderung akan mengalami apoptosis.
Pada trauma otak atau medula spinalis terjadi peningkatan jumlah komplek protein
7

Cyclin D1 dan CDK4 (Cyclin Dependent Kinase-4) yang menginduksi siklus sel
menuju fase G1. Kompleks protein tersebut akan menginduksi fosforilasi Rb
(Retinoblastoma) gen sehingga melepaskan E2F untuk mengaktivasi transkripsi DNA
dan memulai fase S. Fosforilasi Rb gen juga dipengaruhi oleh kompleks Cyclin E/A
dan CDK2 (Cyclin Dependent Kinase-2) pada akhir fase G1. Setelah itu CDK2 akan
terlepas dan berikatan dengan Cyclin B untuk mengawali fase M. Dalam hal ini yang
terpenting adalah E2F dapat menginduksi proses apoptosis baik melalui jalur intrinsik
maupun jalur ekstrinsik. Dengan demikian terjadi peningkatan caspase-3 pada sel-sel
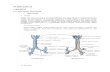
neuron yang menyebabkan apoptosis (Byrnes et al., 2007).
Gambar 1. Proses Kerusakan Neuron (Byrnes et al., 2007)
Proses inflamasi pada susunan saraf pusat diperantarai oleh innate immune
response dan adaptive immune response. Dalam hal ini innate immune response yang
terjadi pada SSP diperankan oleh mikroglia dan astrosit. Mikroglia memiliki reseptor
yang dapat mengenali adanya antigen atau protein stereotipik yang dilepaskan oleh
jaringan saraf pasca trauma. Reseptor tersebut akan mengaktifkan jalur Nucelar
Factor-kappa B (NF-kB) yang memacu pembentukan sitokin proinflamasi seperti
8

TNF-α, IL-1, IL-6, PGE-2 dan NO. Selain itu astrosit juga telah diketahui memiliki
peran dalam respon imun alami dengan mengekspresikan Toll like receptor, Manose
receptor dan Complement receptor yang juga berperan dalam pembentukan sitokin
proinflamasi tersebut. Adapun adaptive immune response diperantarai oleh aktivasi
limfosit pada sirkulasi darah perifer oleh pelepasan sitokin proinflamasi dari SSP.
Limfosit T yang teraktivasi berupa CD4 dan CD8 akan masuk ke SSP melewati sawar
darah otak dan mengeliminasi antigen asing yang terbentuk pada jaringan saraf pasca
trauma. Selain itu sel limfosit CD4 akan mengaktifkan sel limfosit B untuk
membentuk antibodi. Bila terbentuk kompleks antigen-antibodi maka jalur
komplemen akan teraktivasi dan meningkatkan kerusakan selubung myelin (Chen dan
Palmer, 2008; Magnus dan Rao, 2005).
Pada dasarnya sel-sel saraf akan mengalami proses perbaikan pasca trauma
otak dan cedera medula spinalis yang ditandai dengan meningkatnya siklus sel, yang
akan mengatur mitosis neuroblast (Byrnes et al., 2007) . Hal ini diketahui dengan
adanya peningkatan beberapa protein pertumbuhan yang mempengaruhi regenerasi
sel-sel saraf. Beberapa penelitian menunjukkan bahwa protein pertumbuhan tersebut
juga banyak ditemukan pada masa perkembangan awal SSP, protein-protein tersebut
antara lain :
a. GAP-43 (growth-assosiated-protein-43)
GAP-43 adalah membran protein asam yang diekspresikan dalam kadar tinggi
pada saat pembentukan akson dan proses sinapsis antar ujung akson. GAP-43
memiliki substansi serin 41 yang bila difosforilasi dengan PKC-β (protein kinase
C-beta) dapat berikatan dengan kalmodulin sehingga dapat menginduksi
pertumbuhan akson. Ekspresi GAP-43 dapat ditingkatkan oleh beberapa faktor
pertumbuhan seperti FGF-2 (fibroblast growth factor-2), EGF (epidermal growth
factor), IGF-1 (insulin like growth factor-1), CNTF (ciliary neurotrophic factor),
NT-3 (neurotrophin-3) dan NGF (nerve growth factor).
b. PSA-NCAM (polysialylated-neural-cell- adhesion-molecule)
9

PSA-NCAM pada awal perkembangan SSP muncul pada membran sitoplasma
serta puncak pertumbuhan neuron striatal, neuron kortikal dan area hipokampus.
PSA-NCM berfungsi untuk memudahkan interaksi dan interkoneksi antar sel-sel
saraf. Ekspresi PSA-NCAM dapat ditingkatkan oleh beberapa faktor seperti
steroid, serotonin dan NMDA (N Methyl d-Aspartat) receptor ligand (Emery et
al., 2003).
Selain itu telah berhasil diidentifikasi adanya Neural progenitor cell (NPCs)
pada Subventrikular Zone (SVZ) dan Subgranular Zone (SGZ) gyrus dentatus dengan
jumlah yang sangat sedikit. Hal tersebut menunjukkan adanya kemampuan
homeostatis pada SSP orang dewasa dengan memproduksi prekursor sel-sel neuron
untuk menggantikan sel-sel saraf yang telah rusak karena proses apoptosis normal
(Magnus dan Rao, 2005). Tetapi pada keadaan yang patologis, Neural progenitor cell
(NPCs) pada Subventrikular Zone (SVZ) dan Subgranular Zone (SGZ) tidak
mencukupi karena adanya proses inflamasi yang berlebihan (Roth, 2002).
Pada orang dewasa terjadi hambatan dalam proses perbaikan sel saraf pasca
trauma akibat terjadinya inflamasi yang berlebihan. Proses patologis tersebut
menginduksi timbulnya apoptosis yang berlebihan pada area sekitar fokus lesi, baik
melalui jalur intrinsik maupun jalur ekstrinsik. Meskipun proses inflamasi yang
terjadi akan menarik NPC ke lokasi lesi untuk proses regenerasi sel saraf secara
alami, ada beberapa hambatan yang menyebabkan tidak efektifnya migrasi NPC
tersebut, yaitu :
a. Meningkatnya produksi Reactive Oxygen Species (ROS) dan Nitrit Oxide
(NO) pada lokasi inflamasi akan membentuk peroxynitrite yang dapat
merusak komponen intraseluler pada NPCs sehingga menurunkan ketahanan
hidup NPCs.
b. Meningkatnya TNF-α dan Interferon-γ pada lokasi inflamasi akan
menstimulasi ekspresi CD80 dan CD86 pada NPCs yang berasal dari SVG.
Ekspresi CD80 merupakan kostiumulator yang dapat mengaktivasi limfosit T
sitolitik untuk melisiskan NPCs.10

c. Produksi TNF-α, FAS ligand dan TRAIL pada lokasi inflamasi akan
menginduksi proses apoptosis melalui jalur ekstrinsik pada sel neuron dan
oligodendrosit yang terbentuk dari NPCs.
d. Produksi Interleukin-6 (IL-6) yang tinggi pada lokasi inflamasi akan
menghambat proses diferensiasi NPCs menjadi sel neuron melalui sinyal yang
diperantarai gp130 dan meningkatkan diferensiasi astrosit pada jalur mitogen
activated protein kinase (MAPK) (Chen dan Palmer, 2008).
Selain itu pasca trauma sel saraf, kemampuan regenerasi akson menjadi sangat
berkurang. Salah satu mekanisme molekuler yang mendasari keterbatasan
pertumbuhan akson pasca trauma sel saraf adalah penghambatan oleh debris myelin
dan oligodendrosit. Beberapa debris myelin yang berperan menghambat proses
regenerasi akson antara lain : NogoA, MAG (Myelin-Assosiated Glicoprotein), OMgp
(Oligodendrocyte Myelin glicoprotein), Sema4D/CD100 (Semaphorin 4D) dan
Ephrin B3 (Yiu et al., 2006). Di samping itu keterbatasan regenerasi akson juga
disebabkan oleh reaksi pembentukan glial scar yang melibatkan mikroglia dan
astrosit. Proses pembentukan glial scar tersebut dipengaruhi oleh ekspresi IL-1 dan
Interferon-γ serta pelepasan GFAP (Glial Fibrilary Acidic Protein) oleh astrosit dari
jaringan saraf yang normal menuju jaringan saraf yang terkena trauma. Kumpulan
astrosit yang reaktif dan hipertrofik akan mengeluarkan molekul matriks ekstraseluler
berupa CSPGs (Condroitin Sulphate Proteoglycans). Beberapa jenis CSPGs seperti
aggrecan, brevican, neurocan, versican dan phosphacan yang membentuk glial scar
berperan sebagai penghalang mekanik pada proses regenerasi akson. Dengan
demikian renegerasi sel saraf pasca trauma merupakan hal yang sulit dilakukan secara
otonom oleh sistem homeostasis pada SSP (Chen dan Palmer, 2008; Yiu et al., 2006).
3. Stem Cell
a. Definisi
Stem cell merupakan sel yang belum berdiferensiasi dan mempunyai
potensi untuk berdiferensiasi menjadi jenis sel lain (Drucker, 2004). Selama tahap
perkembangan awal sel berbagai tipe stem cell akan mengalami spesialisasi dan 11

diferensiasi menjadi sel dengan fungsi yang lebih spesifik (Goldman, 2006).
Berdasarkan hal tersebut, dilakukan berbagai penelitian untuk menginduksi stem
cell yang belum berdeferensiasi menjadi sel yang spesifik secara fungsional,
sehingga stem cell dapat menjadi salah satu alternatif untuk terapi pengganti sel
yang hilang atau rusak (Rosada et al., 2003).
b. Klasifikasi stem cells
Sampai saat ini telah diidentifikasi empat tipe stem cell berdasarkan
kapasitasnya untuk berdiferensasi menjadi sel lain, yaitu sel totipoten, pluripoten,
multipoten, dan unipoten. Adapun jenis stem cell yang saat ini telah
dikembangkan dalam penelitian antara lain embryonic stem cell, adult stem cell,
dan HUCB stem cell (Maslov et al., 2004). Embryonic stem cell merupakan sel
yang didapatkan dari inner mast cell pada blastosit dan bersifat pluripoten
sehingga dapat berdiferensiasi menjadi semua tipe sel dalam tubuh. Adult stem
cell didapatkan dari jaringan tertentu dalam tubuh yang telah berdiferensiasi. Sel
induk yang berasal dari sel dewasa mempunyai kemampuan diferensiasi yang
terbatas (Sanchez, 2002; Nayak, 2008). HUCB stem cell didapat dari darah tali
pusat yang belum dipotong saat bayi lahir, tipe stem cell ini bersifat pluripoten
dan dapat berdiferensiasi menjadi semua tipe sel dalam tubuh (Saporta et al.,
2003). Berikut adalah bagan klasifikasi stem cell (Maslov et al., 2004).
12

c. Human umbilical cord blood stem cell
Human umbilical cord blood stem cell (HUCB stem cell) termasuk adult
stem cells jika dibandingkan dengan stem cell dewasa lainnya yang berasal dari
susmsum tulang maupun darah tepi. Umbilical cord blood mengandung sejumlah
stem cell yang bermakna dan memiliki keunggulan daripada stem cell yang
diperoleh dari sumsum tulang atau darah tepi. Penggunaan HUCB stem cell
merupakan pilihan yang paling aman dan jika dibandingkan dengan penggunaan
embryonic stem cell yang sering terbentur masalah bioetika. Pada prinsipnya
human umbilical cord blood stem cell merupakan sel yang mempunyai
kemampuan untuk berdiferensiasi tanpa batas menjadi sel jenis lain. Kemampuan
tersebut, memungkinkan stem cell memperbaiki kerusakan tubuh dengan
menyediakan sel-sel baru untuk memperbaiki kelainan tersebut (Zigova et al.,
2002; Simper et al., 2002; Nayak, 2008).
Beberapa penelitian menyatakan bahwa transplantasi stem cell ini dapat
menyembuhkan beberapa penyakit antara lain leukemia, thalasemia, anemia,
myeloma, hodgkin, penyakit jantung, diabetes, systemic lupus erithematosus,
stroke, alzheimer, dan parkinson (Krisiukeniene et al., 2003; Ooi J. et al., 2001).
Stem cell yang berasal dari darah tali pusat ini tidak hanya dapat digunakan oleh
pemiliknya, tetapi juga dapat digunakan oleh saudara kandung ataupun orang tua
pemilik umbilical cord blood tersebut, dengan syarat terdapat kecocokan dalam
struktur gen dan golongan darah. Bila dimanfaatkan oleh saudara kandung,
tingkat kecocokannya mencapai 50-70%. Sedangkan bila digunakan oleh orang
tua, kecocokannya mencapai 50% (Lee et al., 2002; Willing et al., 2003; Nayak,
2008).
Human umbilical cord blood stem cell mempunyai sejumlah keunggulan
dibandingkan dengan sumber stem cell lainnya, antara lain :
a. Pengambilan stem cells ini bebas risiko rasa sakit dan proses pengambilannya
relatif cepat
b. Umbilical cord blood stem cells selalu siap digunakan kapan saja melalui
penyimpanan dalam kulkas cryogenic sampai -1800C13

c. Rendahnya risiko Graft versus Host Disease (GvHD)
d. Kelebihan umbilical cord blood lainnya berhubungan dengan kecocokan
HLA (human leukocyte antigen). Pada transplantasi umbilical cord blood ini
hanya mensyaratkan minimal tiga HLA saja yang cocok. (Terskikh et al.,
2001; Tezuka, 2002; Wichterle, 2002)
Namun stem cell dalam umbilical cord blood memiliki kelemahan
karena jenisnya lebih primitif dibandingkan dengan yang ada di sumsum tulang
belakang sehingga proses penyatuannya memerlukan waktu yang lebih lama. Hal
tersebut membuat penerima transplantasi berisiko tinggi untuk terkena infeksi.
d. Diferensiasi Human umbilical cord blood stem cells menjadi Sel Saraf
Chen et al (2005) telah mengidentifikasi terdapatnya dua subfraksi
dalam fraksi mononuklear umbilical cord blood stem cell. Dua subfraksi tersebut
adalah subfraksi adherent yaitu suatu subfraksi yang mengekspresikan antigen
hematopoetik dengan limfosit sebagai komponen utama (53%) serta subfraksi
floating yang dapat mengekspresikan neuronal antigen. Fraksi mononuklear yang
berasal dari HUCB stem cell mengandung sejumlah sel progenitor yang dapat
berdiferensiasi menjadi beberapa jenis sel tubuh termasuk sel mesenkim dan sel
saraf (Goldman, 2006; Nayak, 2008).
Sebuah studi yang dilakukan oleh Nayak (2008) menyebutkan bahwa
fraksi floating dalam HUCB stem cells dapat mengekspresikan protein neural
yang ditunjukkan dengan tingginya ekspresi reseptor neurotropin trkB dan trkC.
Berdasarkan pemikiran ini dapat diperoleh sel progenitor neuron yang berasal dari
HUCB stem cell dengan teknik purifikasi slow sedimentation. Teknik purifikasi
ini dapat dilakukan dengan mengeliminasi fraksi adherent yang mengekspresikan
antigen hematopoetik dan mengoptimalkan viabilitas fraksi floating dalam
mengekspresikan protein neural secara in vitro (Lee et al., 2002; Goldman, 2006;
Mikami et al., 2002).
Beberapa penelitian telah menggunakan berbagai media dan growth
faktor untuk menginduksi stem cells menjadi sel saraf, antara lain Retinoic Acid
14

(RA), Nerve Growth Factor (NGF), Brain Derived Nerve Factor (BDNF), dan
Endothelial Growth Factor (EGF) (Edling et al., 2004; Lee et al., 2002;
Wichterle, 2002). Kultur mononuklear HUCB stem cells pada medium berisi
serum yang diinduksi dengan RA dan BDNF dilakukan selama 20 hari untuk
mendapatkan sel saraf, astrosit, dan oligodendrosit matur. Pada penelitian ini
digunakan kombinasi RA sebagai growth factor yang dapat menginduksi berbagai
sel ektodermal dan BDNF sebagai growth factor spesifik bagi pembentukan sel
saraf dengan tujuan untuk mengoptimalisasi lingkungan in vitro bagi
pertumbuhan sel multipoten menjadi sel saraf. Dalam penelitian ini dilakukan
analisis komparasi morfologi dan ekspresi antigen spesifik pada hari ke 1, 5, 10,
dan 20 kultur. Penelitian tersebut melaporkan terdapatnya ekspresi nestin tertinggi
sebagai marker utama sel saraf pada hari ke-5 (Goldman, 2006; Nayak, 2008). Di
lain pihak, Sohur (2008) melapokan bahwa dalam 30 hari kultur fraksi floating
dari HUBC stem cells, didapatkan ekspresi protein neural sejak hari pertama.
Sebuah studi melaporkan bahwa pada kultur fraksi floating HUBC stem cells
selama 25 hari didapatkan ekspresi kadar nestin tertinggi setelah hari pertama
kultur sampai hari ke-5 kultur dan ekspresi nestin ini terus menurun setelah 15
hari kultur. Pada kultur ini didapatkan pula kadar GFAP tertinggi pada hari ke-20
kultur, kadar trKc mulai meningkat pada hari ke-10 kultur, dan ekspresi TuJ1
mulai hari pertama kultur (Lee et al., 2002; Wichterle, 2002)
Sebuah studi menunjukan bahwa fraksi floating dari kultur
mononuklear HUCB stem cells didapatkan setelah 20 hari in vitro. Dalam studi ini
didapatkan peningkatkan ekspresi protein neuronal mulai 24-48 jam kultur setelah
diinduksi dengan NGF. Dalam penelitian ini digunakan NGF sebagai suatu
growth factor yang cukup kuat dan spesifik untuk menginduksi pembentukan sel
saraf. Selain itu, NGF merupakan suatu faktor pertumbuhan bagi sel saraf yang
dapat meningkatkan pembentukan dan pematangan NPC secara in vivo. Dalam
studi ini dilakukan analisis tingkat ekspresi protein neural secara kualitatif dan
kuantitatif dengan skala ordinal 0-4 yang dinilai dengan membandingkan
intensitas warna pada setiap lapang pandang pengamatan, dengan penjelasan
15

sebagai berikut 0 : tidak ada ekspresi; 1: intensitas pewarnaan minimal; 2 :
intensitas pewarnaan moderate; 3 : intensitas pewarnaan tinggi; 4 : intensitas
pewarnaan maksimal.Berdasarkan analisis ekpresi tersebut dilaporkan bahwa
fraksi floating berekspresi kuat terhadap antibodi nestin pada hari pertama kultur,
ekpresi TuJ1 yang tinggi pada hari ke-5 dan 10, sedangkan ekspresi GFAP
didapatkan tetap rendah sampai hari terakhir kultur (Lee et al., 2002; Goldman,
2006; Wichterle, 2002)
Mikami et al (2002) dan Wichterle (2002) Melakukan kultur
mononuklear HUCB stem cells dengan induksi BDNF, RA, dan NGF selama 190
hari. Pada studi ini dilakukan analisis western blot terhadap ekspresi protein
neural dengan sel otak hewan coba sebagai pembandingnya, dalam analisis ini
didapatkan ekspresi marker sel saraf yang ditunjukkan pada gambar berikut:
Gambar 1. Ekspresi nestin tinggi pada hari ke-0, ke-5, dan ke-10 kultur,
ekspresi GFAP tinggi pada hari ke-5 kultur, eksprei TuJ1 tinggi pada
hari ke-190 kultur, dan ekspresi A2B5 yang tinggi pada hari ke-190
kultur (Mikami et al., 2002).
16

Berikut adalah beberapa marker yang telah digunakan dalam
berbagai penelitian untuk menunjukkan keberhasilan induksi stem cells
menjadi sel saraf:
Tabel 1. Marker Penanda Sel Saraf (Chen et al., 2005)
Antigen Species Cross Reactivity Dilution
HematopoeticCD133CD117CD15CD45Early NeuralNestinVimentinA2B5NeuronalTuJ1NF68KDMAP2NSEGliaGFAPS100Ga1CReceptorstrKAtrKBtrKCp75NTRCXCR4
MouseMouseMouseMouse
MouseMouseMouse
RabbitRabbitMouseRabbit
RabbitRabbitRabbit
RabbitRabbitRabbitMouseRabbit
HumanHumanHumanHuman
HumanHumanHuman, rat
MamalsRat, human, bovineHuman, rat, mouseHuman
Human, cowHuman Human, animal
HumanHuman HumanHumanHuman
1:501:501:501:50
1:1001:2001:200
1:1,0001:5001:1,5001:100
1:8001:1671:150
1:5001:2,0001:2,0001:4001:1,000
Sebuah studi melaporkan bahwa keberhasilan diferensiasi secara in vitro
dapat ditunjukkan dengan marker penanda sel progenitor neural antara lain:
a. Glial Fibrilary Acidic Protein (GFAP) merupakan marker penanda sel yang
menunjukkan adanya pertumbuhan neuroglial yang mengindikasikan proses
pembentukan sel-sel neuron matur. Reaksi Imunositokimia positif pada protein
spesifik ini menunjukkan kemampuan sel tersebut untuk berkembang menjadi 17

astrosit, oligodendrosit, dan sel glial lainnya (Nassenstein et al., 2003; Willing
et al., 2003).
b. Tyrosin-kinase-C (trKC) merupakan salah satu reseptor yang memperantarai
beberapa fungsi protein yang berefek neurotropik seperti BDNF (Brain Deriver
Nerve Factor) dan NT-3 (Neurotropin 3) yang berperan penting dalam
transdiferensiasi sel progenitor neuron menjadi sel saraf. Reaksi
imunositokimia positif terhadap antibodi trKC pada kultur stem cell
mengindikasikan kemampuan sel tersebut untuk diinduksi menjadi sel saraf
dan beradaptasi dalam lingkungan yang neurogenik (Wichterle, 2002; Zigova
et al., 2002).
c. Nestin, suatu protein neurofilamen yang merupakan marker paling spesifik
dalam pembentukan neural progenitor stem cell yang bersifat multipoten.
Ekspresi nestin banyak ditemukan pada awal perkembangan neurogenesis,
pasca trauma otak dan medula spinalis serta pada pertumbuhan tumor sel saraf.
Pewarnaan imunositokimia positif terhadap antibodi nestin menunjukkan
kemampuan stem cell tersebut untuk berdeferensiasi menjadi sel saraf
(Gilyarov, 2008 ).
d. TuJ1, suatu protein anti β III tubulin yang merupakan marker penanda sel
saraf. Reaksi positif imunositokimia terhadap antibodi TuJ1 menunjukkan
kemampuan stem cell untuk berdiferensiasi menjadi sel saraf.
18

Berikut ini adalah hasil analisis imunositokimia terhadap UCB stem cells
setelah diinduksi dengan BDNF:
Gambar 2 . Immunostaining Terhadap Sel Darah Tepi yang Menunjukkan Hasil
Diferensiasi In vitro HUCB stem cells Menjadi Sel Saraf (Sohur,
2008). Gambar A,E,I menunjukkan early neoronal cell sebagai hasil
diferensiasi HUCB stem cells yang diidentifikasi dengan antibodi
nestin staining. Gambar B,C,D menunjukkan sel saraf sebagai hasil
diferensiasi HUCB stem cells in vitro yang diidentifikasi dengan
neuron-specific immunostaining untuk tubulin tipe IIIb menggunakan
antibodi TuJ1. Gambar F,G,H menunjukkan astrosit sebagai hasil
diferensiasi HUCB stem cells in vitro yang diidentifikasi dengan
Astrocyte-specific immunostaining dengan antibodi GFAP. Gambar
J,K,L menunjukkan ekspresi protein neurotropik pada HUCB stem
cells in vitro yang diidentifikasi dengan antibodi trKC (Sohur, 2008).
19

4. Neural Progenitor Cell (NPC)
a. DefinisiNeural stem cell (NSC) merupakan sel multipoten yang memiliki
kemampuan self renewal dan berespon terhadap sinyal diferensiasi.
Diferensiasi stem cell terjadi secara progresif melalui proses pembentukan
dan pembelahan menjadi sel perkusor yaitu neural progenitor cell dengan
kemampuan diferensiasi lebih spesifik. Sel perkusor ini berperan sentral
dalam perkembangan NSC menjadi sel matur dan berdiferensiasi menjadi sel
saraf, astrosit, dan oligodendrosit.
Perbedaan antara berbagai populasi sel progenitor pada susunan saraf
pusat didasarkan atas kemampuan sel progenitor tersebut untuk memproduksi
berbagai macam tipe sel saraf. Sel progenitor neural yang memiliki
kemampuan berdiferensiasi menjadi sel saraf dikenal sebagai neuronal
restricted progenitors (NRPs) sedangkan yang berdiferensiasi menjadi
mikroglia seperti astrosit dan oligodendrosit dikenal sebagai glial restricted
progenitors (GRPs) (Gage, 2003; Yang et al., 2000).
Sel progenitor dapat diidentifikasi sebagai NRPs apabila memenuhi
beberapa kriteria berikut: (1) mempunyai kemampuan berproliferasi; (2)
mempunyai kemampuan untuk berdiferensiasi menjadi sel saraf walaupun
berada dalam lingkungan dan kondisi yang memacu diferensiasi menjadi sel
glia secara in vitro maupun in vivo; (3) dapat mengekspresikan marker neuron
spesifik, seperti tubulin tipe III, MAP, dan nestin. Selain itu, telah
diidentifikasi bahwa sel progenitor neuron dapat mengekspresikan molekul
adhesi sel saraf yaitu embryonic neuronal adhesion molecule (E-NCAM) dan
PSA-NCAM (polysialylated-neural-cell- adhesion-molecule) (Kokaia et al.,
2004; Suzuki dan Goldman, 2003). Molekul adhesi ini merupakan faktor
yang berperan penting dalam migrasi progenitor sel saraf menuju tempat
kerusakan (Marshal et al., 2003).
20

Sel progenitor diidentifikasi sebagai GPRs apabila memenuhi
kriteria sebagai berikut: (1) mempunyai kemampuan berproliferasi; (2)
mempunyai kemampuan untuk berdiferensiasi menjadi mikroglia walaupun
berada dalam lingkungan dan kondisi yang memacu diferensiasi menjadi sel
saraf secara in vitro maupun in vivo; (3) mengekspresikan marker sel glia
spesifik yaitu GFAP (Pencea et al., 2001; Schubert et al., 2000).
b. Karakterisasi NPC in vivo dan in vitro
Karakterisasi NPCs secara in vitro maupun in vivo didasarkan pada
kemampuan sel tersebut untuk mengekspresikan marker sel saraf dan sel glia
spesifik, sedangkan sel saraf imatur tidak mempunyai kemampuan
mengekspresikan marker tersebut (Bonsall dan Luskin, 2003). NPCs akan
mengekspresikan marker sel saraf dan sel glia spesifik selama fase mitosis
aktif. Pada kultur sel progenitor neural secara in vitro, didapatkan ekspresi
nestin pada hari pertama kultur, ekspresi tubulin tipe III pada hari ke-6 kultur,
dan ekspresi MAP-2 sebagai penanda sel saraf matur. Selain itu, pada tahap
awal kultur diekspresikan marker sel glia spesifik, GFAP dan molekul adhesi
E-NCAM (Nguyen et al., 2004).
Secara klinis NPCs dapat ditransplantasikan secara invasif maupun
non invasif. Transplantasi hasil induksi stem cell ini secara invasif dapat
langsung mencapai target organ tetapi berisiko tinggi karena melibatkan
proses pembedahan. Adapun transplantasi non invasif dilakukan melalui
transfusi intravena. Sebuah studi menyatakan bahwa dalam sekali
transplantasi stem cell melalui transfusi intravena direkomendasikan terdapat
minimal 100.000 sel. Akan tetapi transfusi intravena dalam bentuk stem cell
yang belum berdiferensiasi memiliki resiko menimbulkan teratoma. Studi
yang dilakukan oleh Drucker (2004) telah melakukan kultur NPC yang
diambil dari subventrikular zone hewan coba. Dalam studinya, kultur NPC ini
dapat ditransplantasikan kembali pada hewan coba secara intravena dan
21

menunjukkan perbaikan yang nyata pada 8 minggu posttransfusi. Sejalan
dengan Drucker (2004), Horrobin (2002) dan Zigova (2002) menyebutkan
bahwa transfusi stem cell dalam bentuk sel progenitor dapat meminimalkan
terjadinya teratoma. Hal ini berkaitan dengan kemampuan sel progenitor
tersebut untuk beradapatasi dengan lingkungan neurogenik dan kemampuan
diferensiasi yang lebih spesifik (Horrobin, 2002; Zigova et al, 2002; Drucker,
2004).
Secara in vivo, sel progenitor neural tidak bermigrasi secara radial
sepanjang sel glia, tetapi sel progenitor ini mampu memproduksi suatu
substrat untuk mempermudah migrasi menuju lokasi kerusakan sel saraf
melalui mekanisme migrasi berantai (chain migration). Mekanisme ini
berlangsung dalam dua tahap yaitu proses stepping yang melibatkan E-
NCAM sebagai molekul adhesi dan proses homing pada lokasi kerusakan
(adjacent cell) (Maricich et al., 2001). Sel saraf yang mengalami kerusakan
akan mengekspresikan berbagai molekul kemoatraktan yaitu suatu molekul
pengikat E-NCAM pada proses stepping. Sedangkan molekul yang terlibat
pada proses homing sel progenitor neural antara lain sinyal molekul
proteoglikans, NCAM, slit, serta aminobutyric acid-ergic (GABAergic),
melalui proses homing ini sel progenitor akan beradaptasi dan berdiferensiasi
menjadi sel saraf matur (Pencea dan Luskin, 2003; Wang et al., 2003).
Keberhasilan transplantasi stem cell menggunakan metode transfusi
intravena tidak lepas dari pengaruh sinyal biokimia yang terdapat pada sel
target. Sebuah studi menyatakan bahwa sel saraf yang mengalami kerusakan
akan mengekspresikan berbagai atractant molecule seperti retinoic acid (RA)
dan brain derived nerve factor (BDNF) untuk menarik progenitor sel saraf
tersebut ke lokasi kerusakan. Selain itu sel mononuklear yang berasal dari
stem cell ini juga mengekspresikan faktor angiogenik yaitu Vascular
Endothelial Growth Factor (VEGF) serta Angiopoietin 1 dan 2 yang berperan
sebagai mempermudah migrasi sel progenitor neuron menuju lokasi
22

kerusakan sel saraf. Selanjutnya stem cell tersebut akan berdiferensiasi
menjadi sel saraf, astrosit dan oligodendrosit karena paparan RA dan BDNF
di lokasi lesi tersebut (Drucker, 2004; Pencea et al., 2001).
c. Kontrol intrinsik dan ekstrinsik NPC
Sebuah studi menyatakan bahwa kemampuan NPC dalam
menggantikan kerusakan sel saraf berkaitan erat dengan faktor regulasi,
proliferasi, survival, dan diferensiasi. Mekanisme kontrol yang berhubungan
dengan faktor-faktor tersebut yaitu: (1) regulasi intraseluler langsung yang
terlibat dalam cell cycle progression (kontrol intrinsik) dan (2) sinyal
ekstraseluler, yang melibatkan mekanisme diffusible, membrane bound, dan
ECM bound (sinyal ekstrinsik) (Wichterle et al., 2001).
Terdapat beberapa sinyal protein yang berperan meregulasi proliferasi
sNPC, yaitu neuron spesific protein cyclin dependent kinase inhibitors
(CDKIs) yang mengatur proliferasi sebelum fase postmitotik. CDKIs
merupakan regulator sentral yang mengontrol proses progresi selama siklus
pembelahan sel. Pada setiap proses pembelahan, sel akan mengalami empat
fase dalam siklus sel yaitu G1, S, G2, dan M (G=gap, S=sintesis, M=mitosis)
(Sanai et al., 2004). Sinyal ekstraseluler dan intraseluler terlibat dalam
pengaturan proliferasi sel pada fase transisi dari fase G1-S (checkpoint) untuk
mengatur apakah sel tersebut akan membelah atau masuk dalam fase
postmitotik. Dalam hal ini CDKIs berperan sebagai regulator negatif dari
cyclin dependent kinase (CDK) untuk menghentikan siklus sel pada fase G1,
sedangkan CDK4 dan CDK6 merupakan sinyal protein yang berperan dalam
memacu progresivitas siklus sel dari fase G1 ke S (Yang et al., 2000). Studi
yang dilakukan oleh Coskun dan Luskin (2001) melaporkan terdapatnya
ekspresi CDKIs pada kultur NPC secara in vitro, hal ini mengindikasikan
bahwa CDKIs merupakan sinyal intraseluler yang berperan dalam proliferasi
dan mempertahankan NPC agar tetap berada dalam fase postmitotik.
23

Kontrol ekstrinsik proliferasi NPC diperankan oleh sinyal bone
morphogenic proteins (BMPs) yang berfungsi mengontrol cell cycle arrest.
BMPs merupakan kelompok sitokin transforming growth factor yang
berperan dalam mengontrol proliferasi sel (Bonsall dan Luskin, 2005). Kultur
NPCs secara in vitro menunjukkan bahwa BMP4 dapat meningkatkan jumlah
sel yang berekspresi terhadap marker spesifik sel saraf MAP-1 dan tubulin
tipe III. Studi yang dilakukan oleh Sanai et al (2004) menyatakan bahwa
BMPs berperan secara sinergis bersama CDKIs dalam mengatur proliferasi
sel.
Selain itu, kontrol ekstrinsik NPC juga diperankan oleh brain derived
nerve factor (BDNF) suatu neurotropin afinitas rendah. Sebuah studi
menyatakan bahwa BDNF mampu meningkatkan jumlah sel saraf pada
lingkungan neuron, selain itu secara in vitro BDNF mampu meningkatkan
diferensiasi NPC menjadi sel saraf matur dan meningkatkan kemampuan
survival NPCs dalam lingkungan neurogenik. Dalam studi ini diidentifikasi
adanya ekspresi trkC, suatu reseptor tirosin kinase dengan afinitas tinggi
terhadap BDNF (Gage, 2003; Wang et al, 2003).
24

F. Kerangka Berpikir
G. Hipotesis
1. Waktu induksi berpengaruh terhadap ekspresi marker protein nestin, GFAP,
TuJ1, dan trkC pada kultur HUCB stem cell menjadi NPC dengan NGF in vitro.
2. Kadar NGF berpengaruh terhadap ekspresi marker protein nestin, GFAP, TuJ1,
dan trkC pada kultur HUCB stem cell menjadi NPC.
25
Related Documents